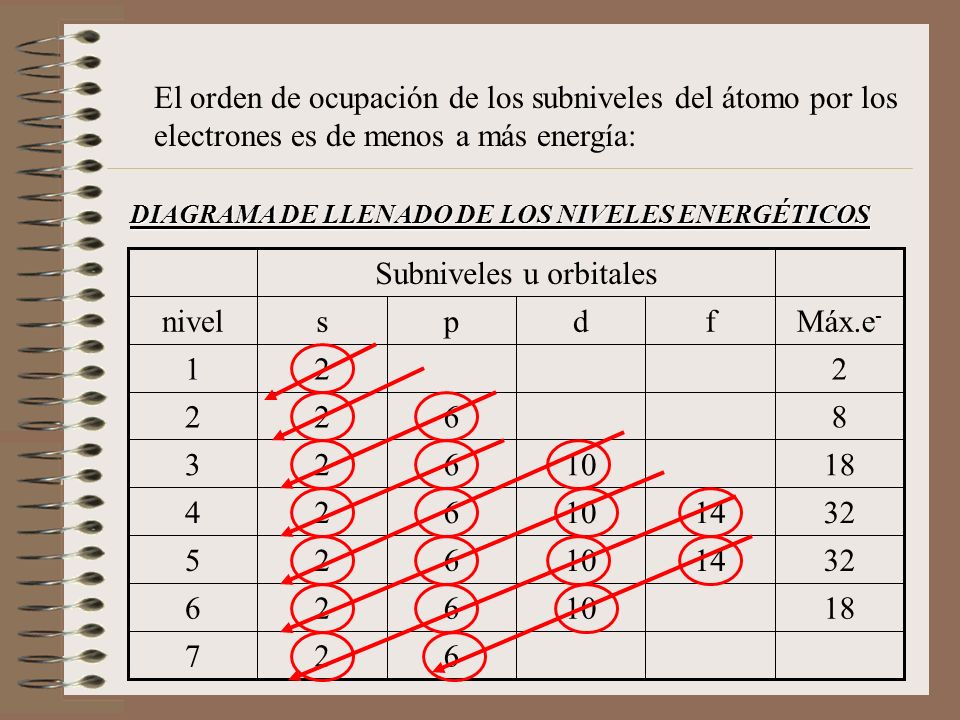
El periodo o nivel de energía del sodio es: 3 . Datos: Na. Z= 11. Explicación: La configuración electrónica de un átomo, es la distribución de los electrones de un átomo en diferentes niveles y subniveles de energía. Con la configuración electrónica podemos determinar:. El nivel de energía principal, también conocido como número cuántico principal, es la región o la capa exterior al núcleo del átomo en la que se puede encontrar un electrón sin perder ni ganar energía y siendo dicha energía la menor posible.Los niveles de energía principales tienen a su vez subniveles de energía. Estos subniveles son conocidos como número cuántico secundario o.

Top 32+ imagen modelo atómico de bohr del sodio Abzlocal.mx
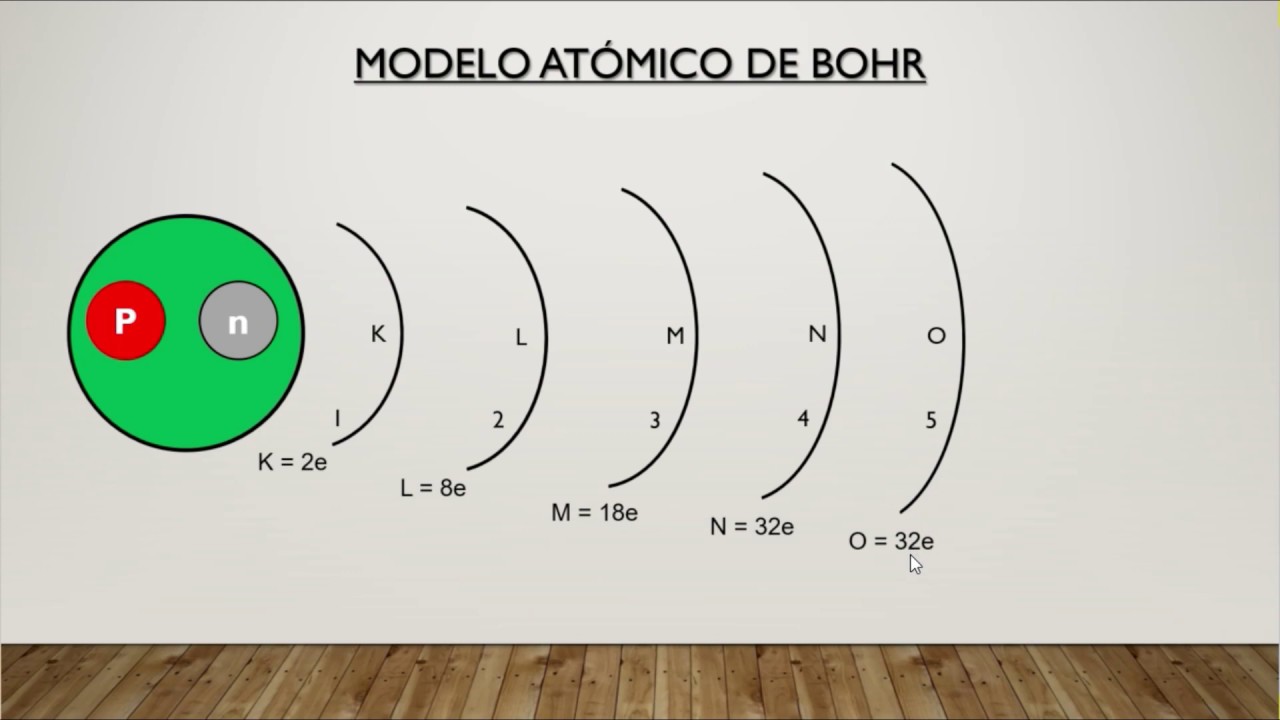
Arriba 57+ imagen modelo atómico de bohr niveles de energía Thcshoanghoathambadinh.edu.vn

Modelo atómico de Bohr del elemento SODIO YouTube

Numeros cuanticos y orbitales atomicos
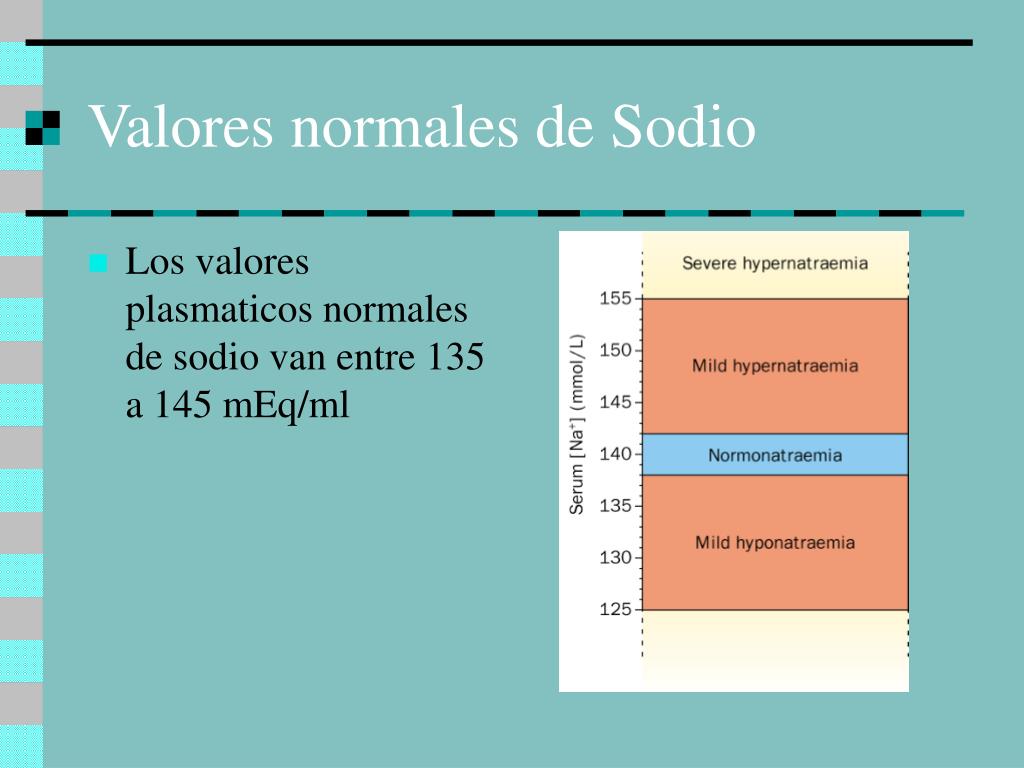
Niveles De Sodio Normales Images and Photos finder

un atomo con tres niveles energeticos Brainly.lat
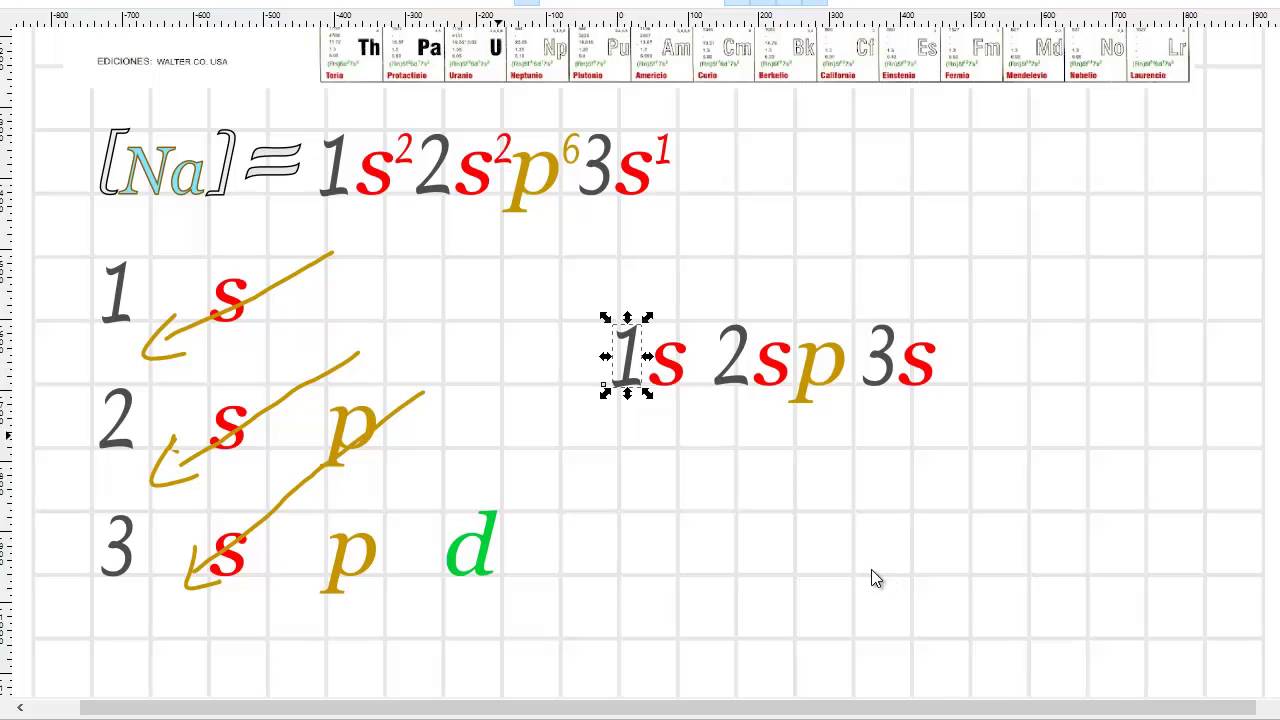
Configuración electrónica del Sodio Cursos Online Web
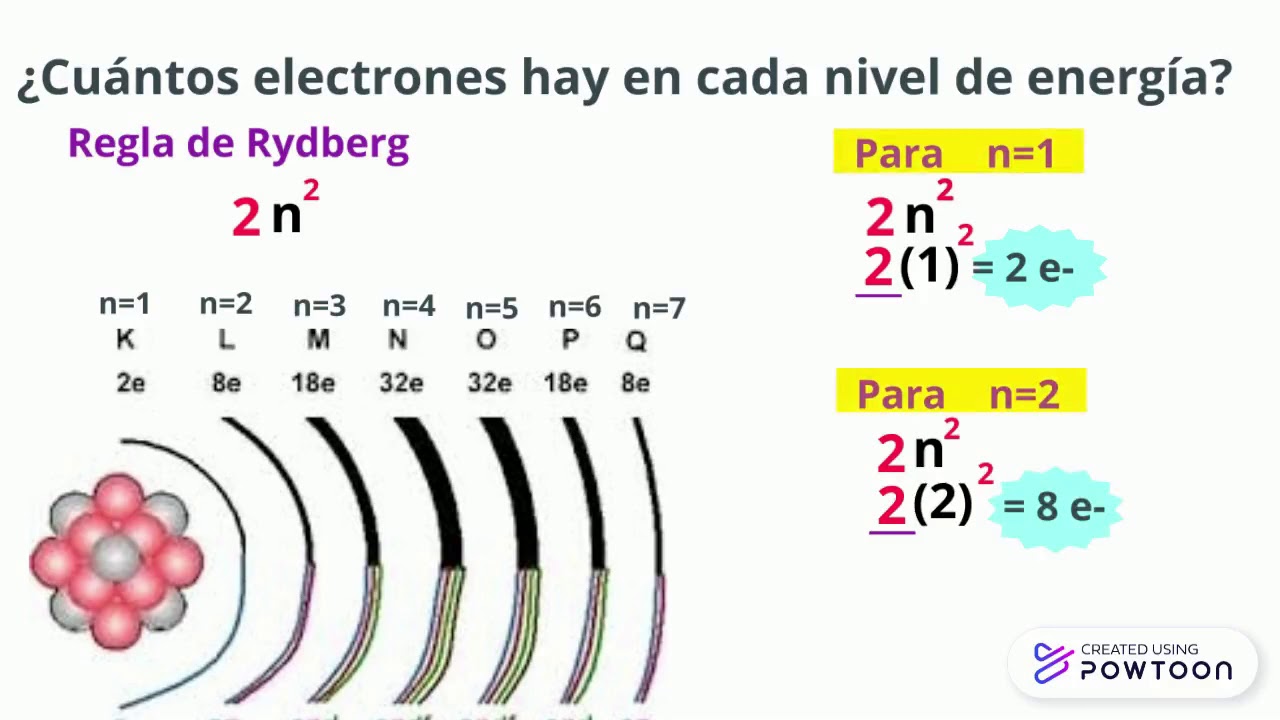
Introducir 67+ imagen modelo de bohr niveles de energía Abzlocal.mx

Porque el símbolo del sodio contiene dos letras, cuantos niveles de energía presenta, cuantos
BIENVENIDS AL MARAVILLOSO MUNDO DE LA BIOLOGÍA 720 NIVELES DE ENERGIA
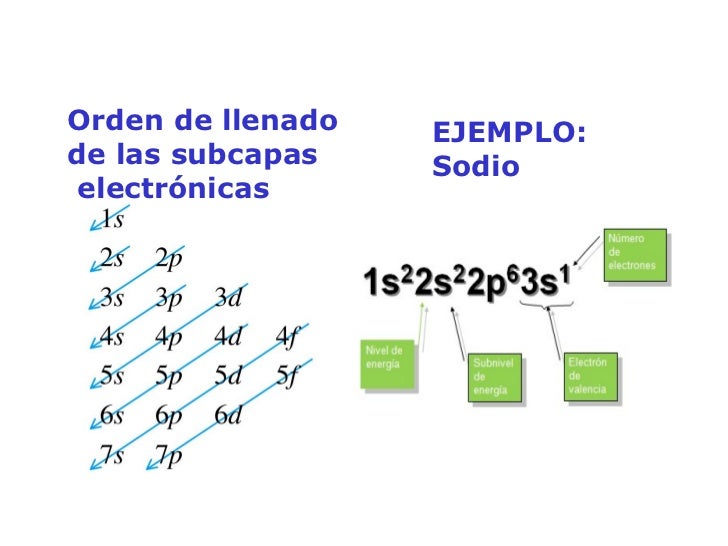
Electrones en niveles de energía

Cuantos Niveles De Energia Hay En La Tabla Periodica
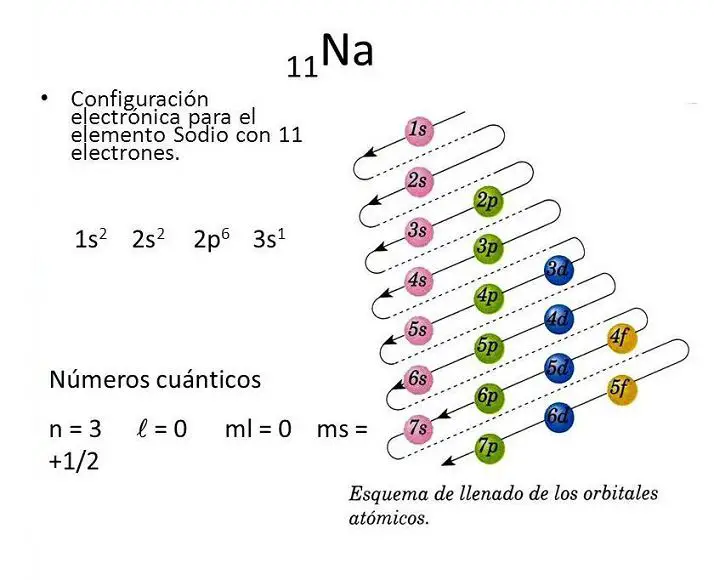
Configuración electrónica del Sodio

Perteneciente al área temática Estructura atómica, este ítem se refiere a las capas o niveles de
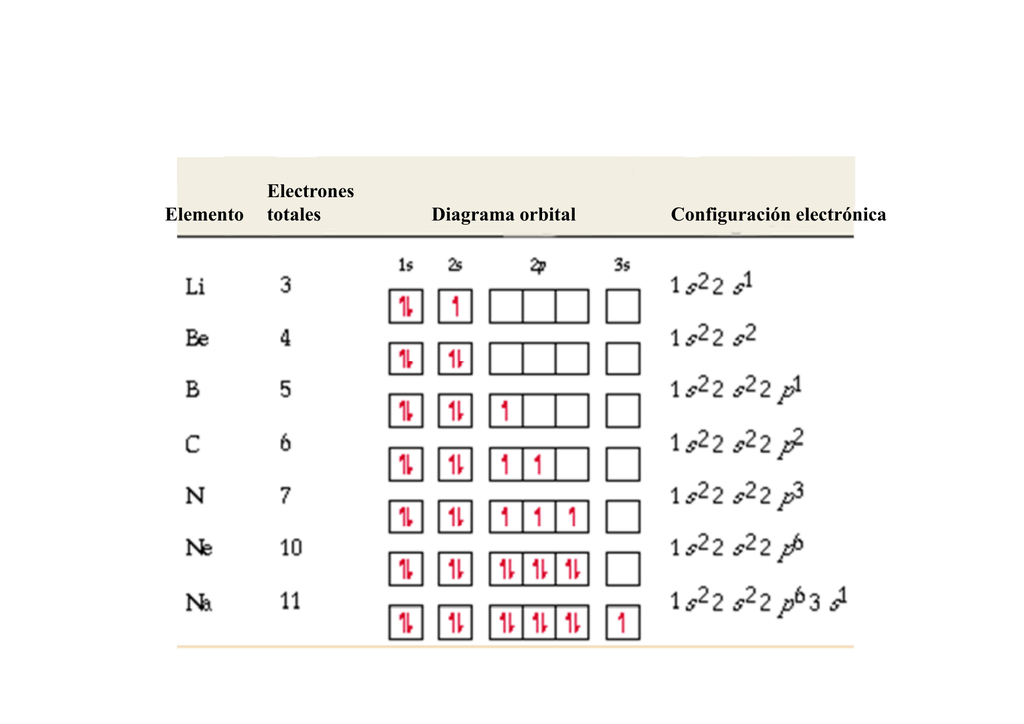
Diagrama De Orbitales De Todos Los Elementos Png Cismos Images And Sexiz Pix
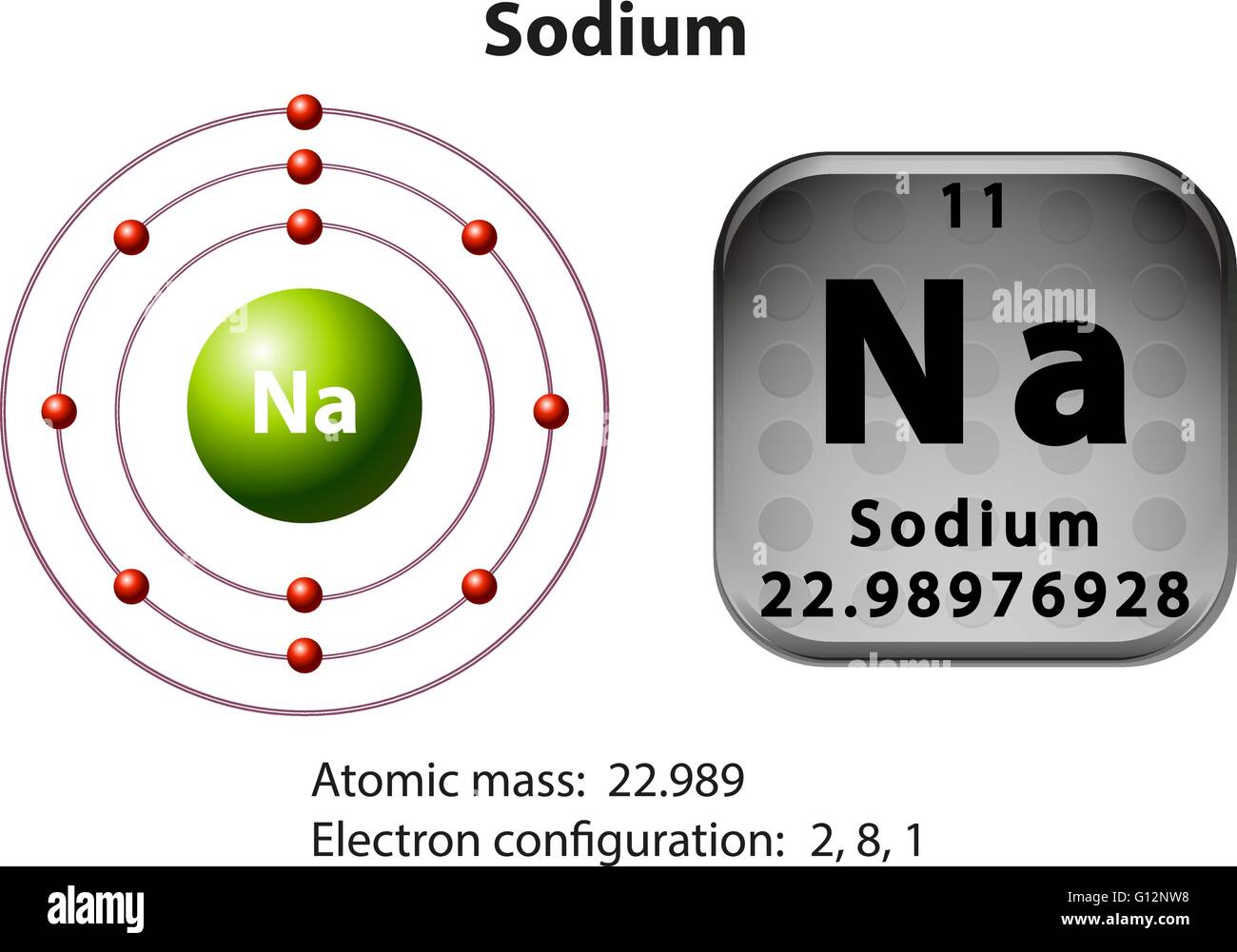
Símbolo y diagrama de electrones para ilustración de Sodio Imagen Vector de stock Alamy
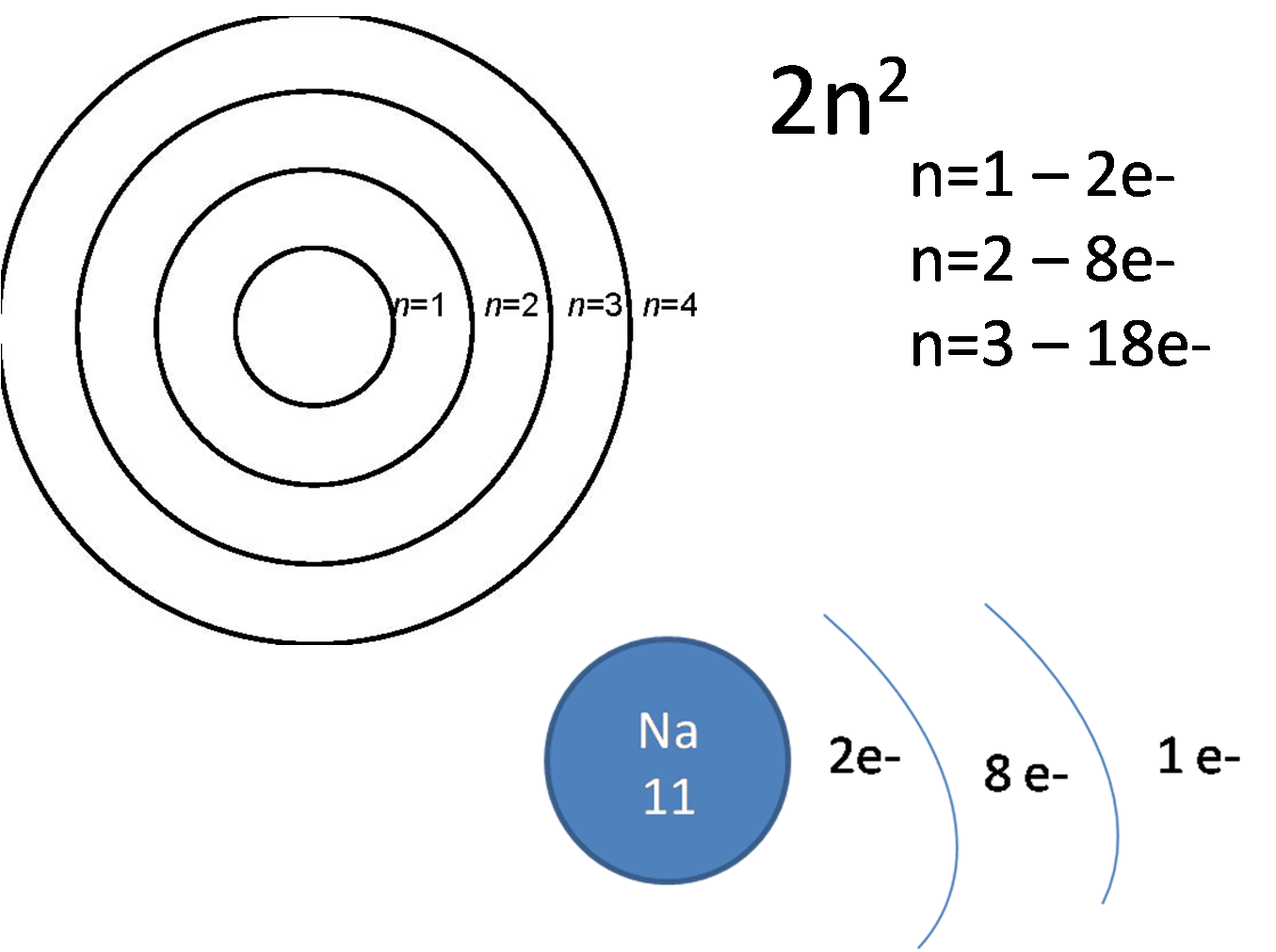
Cuaderno de Ciencias REPASO N°1

Introducir 49+ imagen modelo atómico del sodio Abzlocal.mx
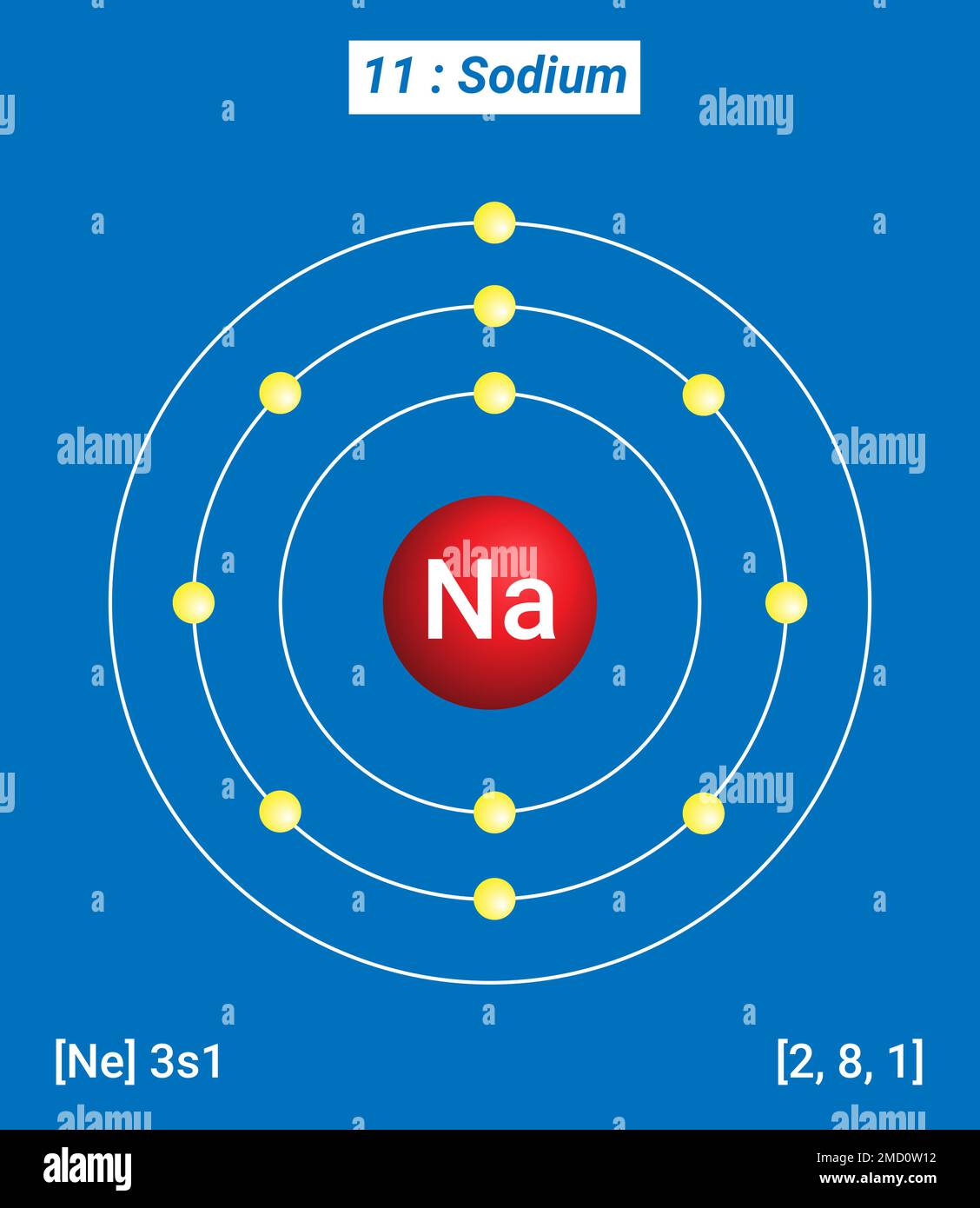
NA Sodio, Tabla Periódica de los Elementos, Estructura de Shell de Sodio Electrones por nivel
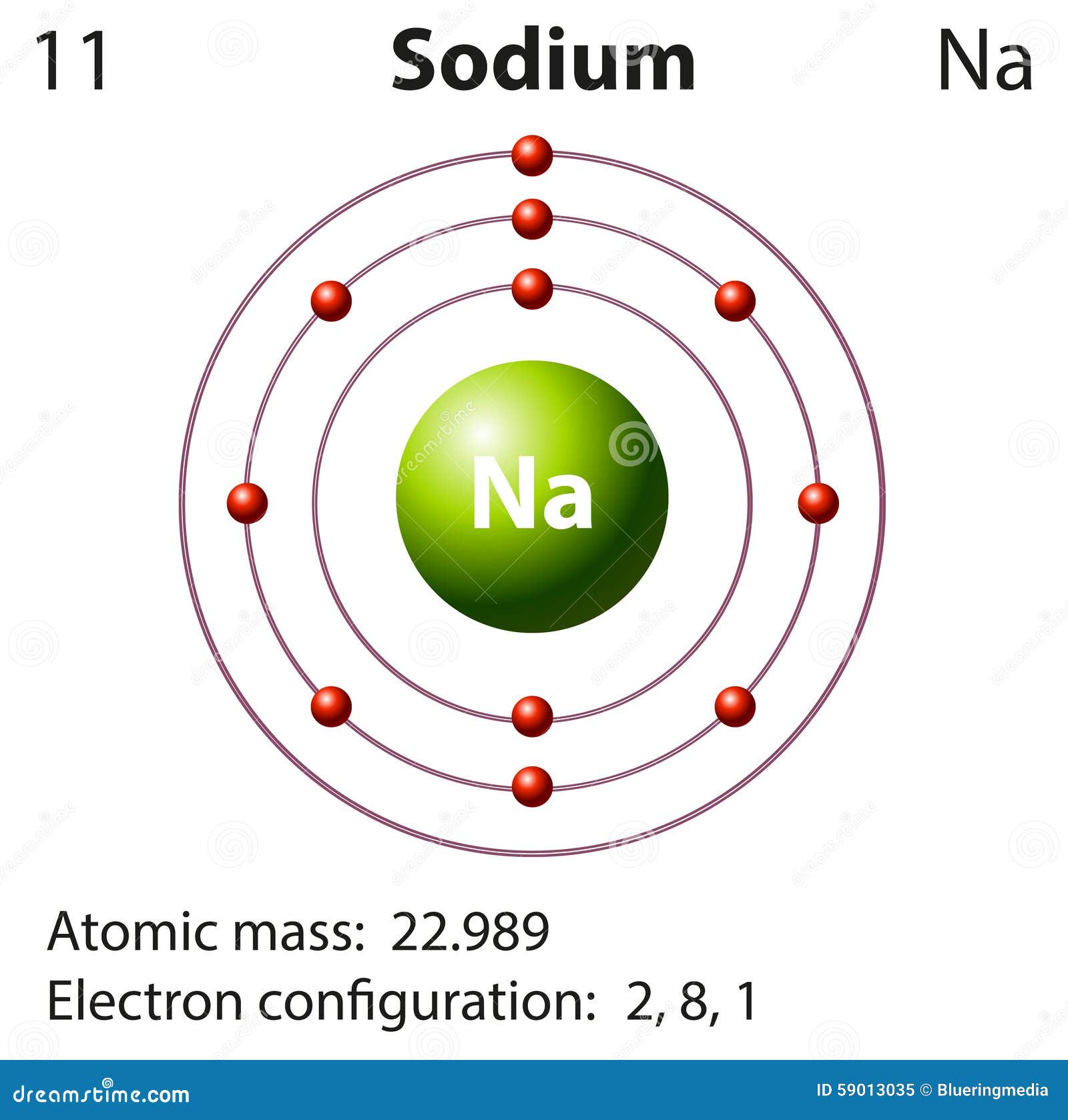
Diagrama De Orbitales Del Sodio Electronica
Espectro del Sodio. El espectro del sodio está dominado por el brillante doblete conocido como líneas-D del sodio, a 588,9950 y 589,5924 nanómetros. En el diagrama de nivel de energía se puede observar que estas líneas son emitidas en una transición desde los niveles 3p a 3s. La línea en 589,0 tiene el doble de la intensidad de la línea.. Ese electrón está en el primer nivel de energía. Los átomos más grandes tienen más electrones. Los electrones siempre se agregan primero al nivel de energía más bajo hasta que tenga el número máximo de electrones posible. Entonces los electrones se agregan al siguiente nivel de energía superior hasta que ese nivel esté lleno, y así.




